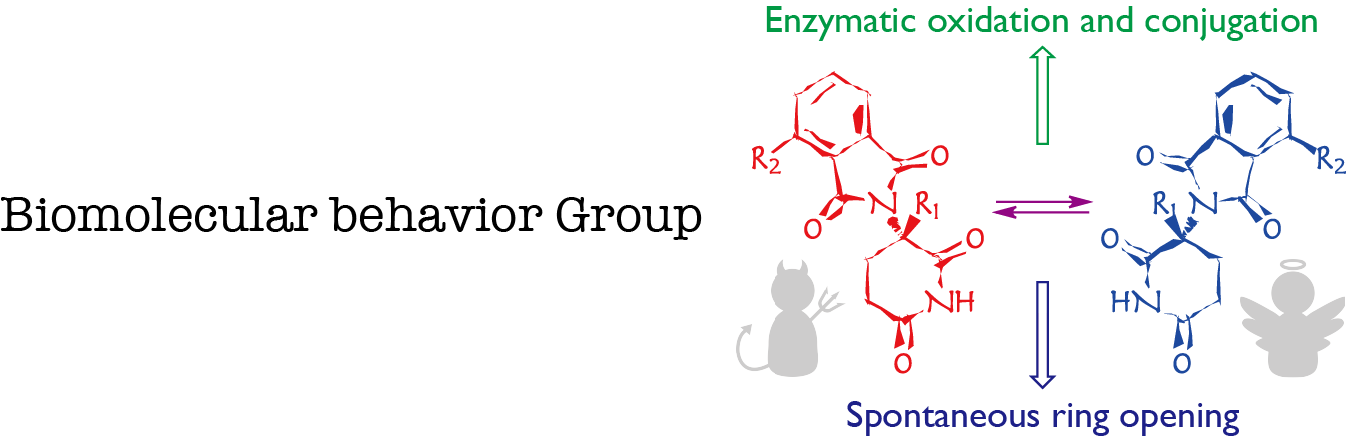
溶液中・固体中におけるキラルな医薬品分子動態の物理化学的解析
キラリティを持つ分子は、食品、農薬、医薬品などさまざまな分野で機能性分子として多く用いられている。特に、医薬品におけるキラリティは受容体との結合の特異性を高め、より有用な薬理作用を生み出すために重要である。我々のグループでは、最近再び注目を集めているサリドマイド及びその誘導体に着目している。
サリドマイドは1957年にドイツで安全な睡眠薬・鎮静薬として開発され、つわりを抑えるために多くの妊婦がサリドマイドを服用したが、やがて手足の発達に異常がある胎児が多く生まれた(アザラシ肢症)。その後、サリドマイドのR体、S体の2つの対掌体(エナンチオマー)のうち、R体には催奇形性は無く、S体のみが催奇形性を引き起こすと報告された。サリドマイドの薬害は、医薬品開発におけるキラリティの識別・分離の重要性を世界に知らしめる大きな契機となった。
だがさらに研究が進むと、生理条件下でサリドマイドはキラル反転を起こし、R体とS体が相互に変換してラセミ化することが報告された。さらにサリドマイドは様々な代謝を受けることが知られており、特に水の存在下では比較的速やかに加水分解され複数の代謝産物が生成する。このように、キラル反転と様々な代謝が組み合わさって同時に起こることで、サリドマイドの詳細な薬理作用メカニズムの解明は非常に困難なものになっている。
作用機序についてまだ未解明な部分が多いサリドマイドだが、近年では多発性骨髄腫、ハンセン病、ベーチェット病、AIDSなど多くの難治性疾患に対する治療薬としての有効性が認められるようになってきた。またサリドマイドの薬理活性を高めるために、さまざまな誘導体・類似体の開発も進んでいる。ごく最近ではサリドマイドの受容体タンパク質としてCereblonが同定され、サリドマイドとの共結晶X線構造解析によって受容体との結合様式が明らかにされた。我々は、歴史的な教訓としてだけではなく、未来への可能性を秘めた新しい医薬品としてサリドマイドを研究することに大きな意義があると考えている。
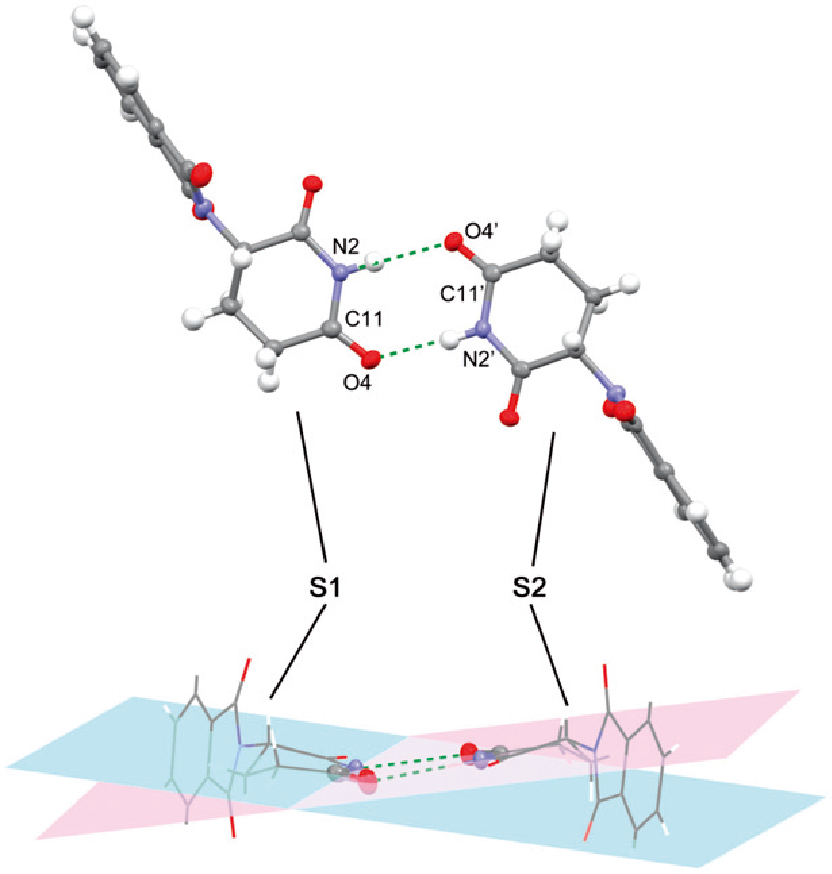
右:図2. 結晶構造中のホモキラルなサリドマイド二量体(文献[1]より作成)
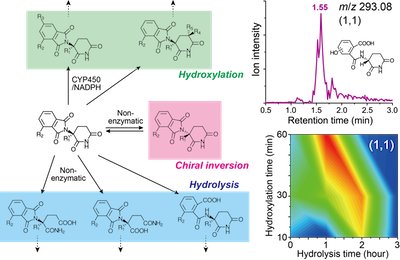
右:図3. 加水分解と酸化を一回ずつ受けたサリドマイド代謝産物のLC-MS/MSによる定量と代謝マップ(文献[2]より作成)
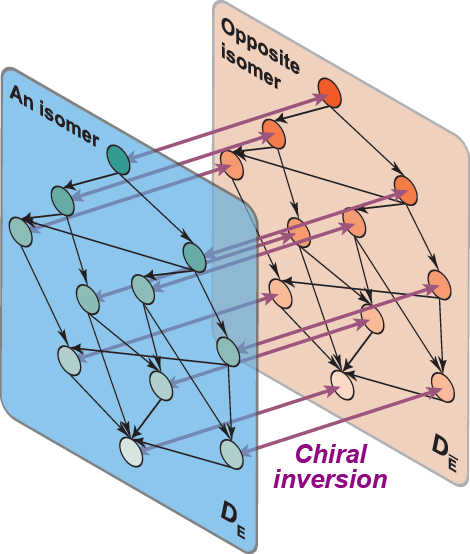
右:図4. キラル反転と代謝の化学反応グラフ(文献[3]より作成)
当研究室ではさらに、キラル分光学、分析化学、結晶光学、熱分析、量子化学計算、数理モデリングなどを用いて、さまざまな角度からのアプローチでのサリドマイドのユニークな性質の解析を以下のように進めている。
(1) サリドマイドとその誘導体のキラル反転と代謝の関連性の解析
(2) サリドマイドの加水分解産物が示す物理化学的性質の測定
(3) 溶液・固体状態におけるサリドマイドの多量体形成の解析
(4) 固相化学反応によるサリドマイド加水分解の逆反応及び熱ラセミ化の解析
参考文献
[1] Suzuki, T. et al. Phase Transition 2010, 83, 223-234.
[2] Ogino, Y. et al. Chirality 2017, in press.
[3] Ogino, Y. and Asahi, T. J. Theo. Biol. 2015, 373, 117-131.
